Почему аминокислотный комплекс Эргамин помогает в восстановлении после инсульта
Инсульт является ведущей причиной инвалидности в мире. Около трети выживших после инсульта остаются инвалидами, а треть не может ходить без посторонней помощи. Реабилитация длительная и заключается в большом количестве физических упражнений.

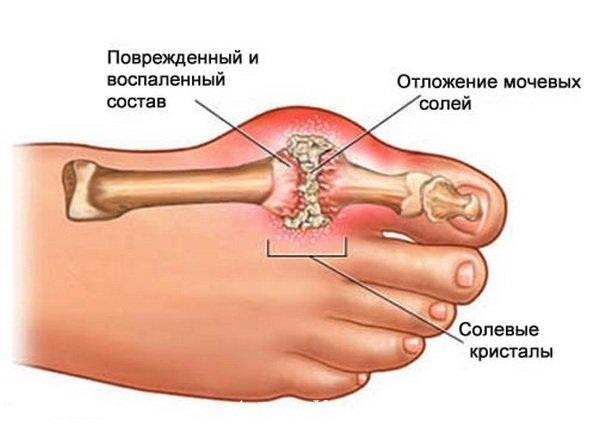
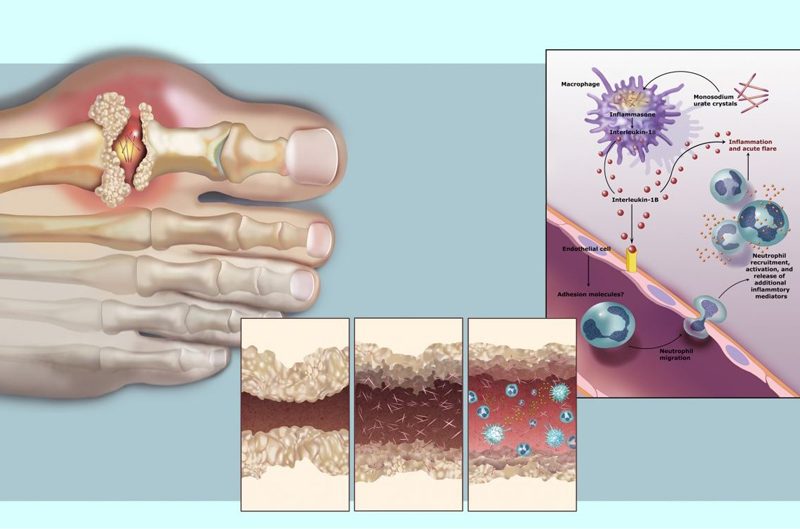
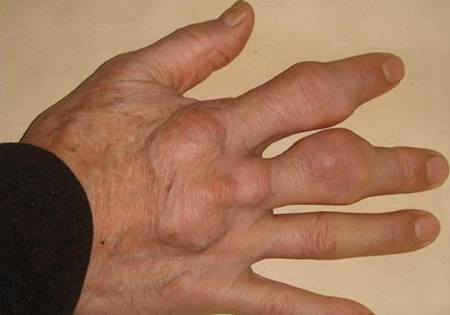
Постинсультные изменения мышц, а именно – увеличение внутримышечного жира, замещающего мышечную ткань – также потенциально могут способствовать инвалидности. То есть в мышцах человека после инсульта из-за стойкого системного воспалительного состояния деградация белка превышает синтез. Что затрудняет физическую реабилитацию.
Исследования группы итальянских ученых, опубликованных в издании «BioMed Research International» доказали, что добавки незаменимых аминокислот способствуют синтезу белка в мышцах и росту мышечной активности организма в целом.
Новый аминокислотный комплекс “Эргамин”, содержащий 18 аминокислот, весьма эффективен при лечении последствий инсульта и последующего периода реабилитации.
✔️ Способствует образованию белка
✔️ Снимает ферментативную недостаточность
✔️ Препятствует белковой анемии
✔️ Поддерживает быстрый рост
✔️ Способствует выведению жира, так как ферменты расщепляют жир
✔️ Помогает худеть и набирать вес, если есть сильное истощение
Все эти свойства Эргамина способствуют эффективности препарата в после-инсультном реабилитационном периоде, когда синтез белка в мышечных тканях жизенно важен для восстановления опорно-двигательного аппарата больного.
Препарат защищен патентом РФ. Правообладатель – профессор биохимии Эрик Тер-Саркисян. Сертифицирован на территории России и Европейского экономического союза.